محرکهای ژنی کریسپر (CRISPR) به دانشمندان اجازه میدهند تا توالیهای DNA را تغییر دهند. کریسپر ابزاری برای بریدن و چسباندن محرکهای ژنی است که پژوهشگران با استفاده از آن DNA را ویرایش میکنند. هماکنون، پژوهشگران از فناوری مشابهی به نام محرکهای ژنی (gene drive ) استفاده میکنند. این فناوری تضمین میکند صفات ژنتیکی ویرایش شده توسط نسلهای آینده به ارث خواهند رسید. فرآیند محرکهای ژنی کریسپر تغییر گونههای زنده مختلف را برای همیشه امکانپذیر میکند. با این حال این پرسش ایجاد میشود که فناوری قدرتمند محرکهای ژنی چه تاثیری بر بشریت دارد؟ از آن برای چه تغییری استفاده خواهیم کرد؟ این فناوری در چه زمینههایی کاربرد دارد؟ جنیفر کان (Jennifer Kahn) روزنامهنویس در سخنرانی TED به این پرسشها پاسخ خواهد داد. با مجله فناوریهای توانافزا و پوشیدنی همراه باشید.
از کاربردهای این فناوری میتوان تولید پشههای مقاوم در برابر مالاریا را نام برد که بیماری مالاریا را ریشهکن میکنند. این بیماری از پشه به انسان منتقل میشود. بیست سال پیش، زیستشناسی به نام آنتونی جیمز (Anthony James) ایده پشههای مقاوم در برابر مالاریا را بیان کرد، یعنی پشههایی تولید کند که دیگر بیماری مالاریا را انتقال نمیدهند. ایده او بسیار عالی بود اما در آن زمان با شکست مواجه شد. چند سال پیش آنتونی جیمز با افزودن برخی ژنها به پشهها باعث شد انگل مالاریا نتواند در بدن پشه زنده بماند. بنابراین دانشمندان توانستند با تغییر ژن پشه، آن را در برابر انگل مالاریا مقاوم کنند. با حل مشکل پشههای ناقل مالاریا، با مسئلهای دیگر روبرو خواهیم بود. چگونه ژنهای همه پشههای ناقل مالاریا را تغییر دهیم؟ چند راهکار وجود دارد.
راهکار نخست: پرورش دادن پشههای با ژنهای تغییر یافته و رها کردن آنها در طبیعت، به امید اینکه پشههای مقاوم در برابر مالاریا گسترش یابند. مشکل این روش این است ده برابر پشههای بومی باید پشههای مهندسی ژنتیکی شده در طبیعت رها شود.
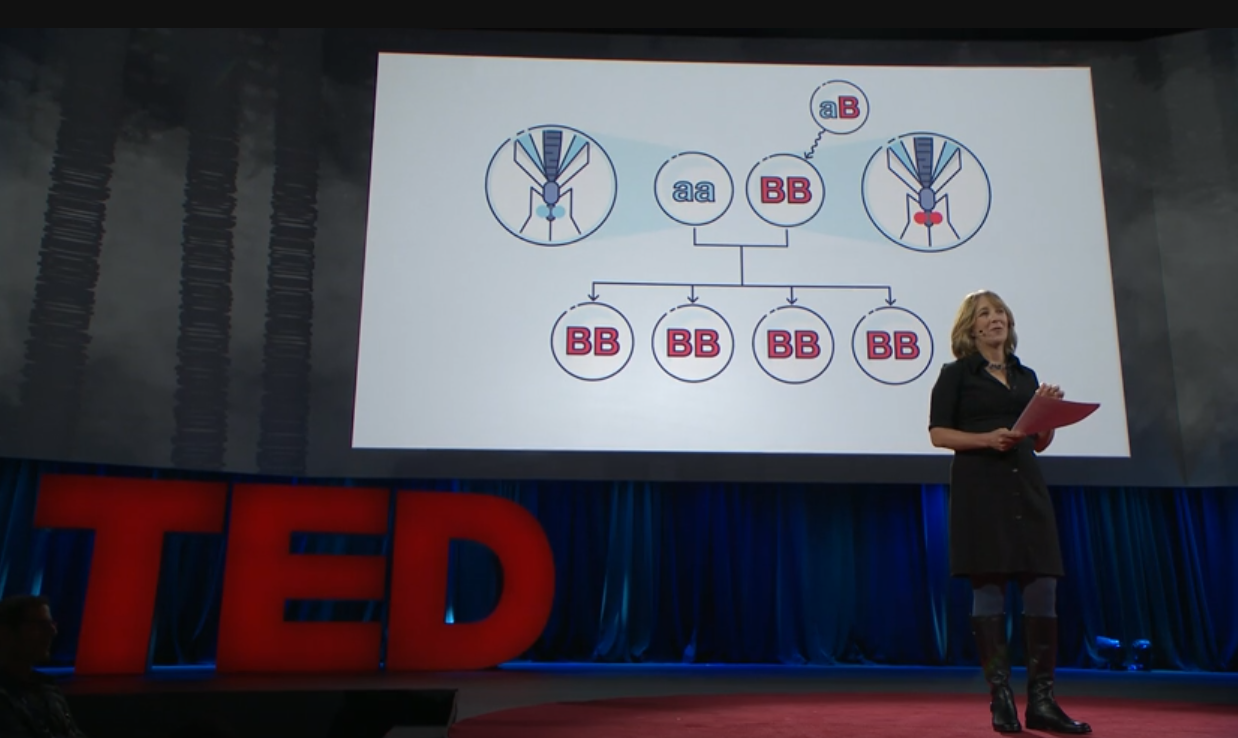
راهکار دوم: ابزاری به نام محرکهای ژنی (gene drive) توسط زیستشناسان کشف شده است که باعث میشود تنها یک صفت ژنتیکی خاص توسط موجود زنده به ارث برده شود. با این روش گسترش ژن با سرعت بیشتری انجام میشود. اگر این روش عملی شود موضوعی که از بیست سال پیش تاکنون مورد مطالعه قرار گرفته حل میشود. در یک آزمایش دو پشه، حامل ژنهای ضد مالاریا شدند و همچنین محرکهای ژنی روی آنها اعمال شد.
در این آزمایش، هر پشهای که ژن مقاوم در برابر مالاریا داشت، رنگ چشمهای آنها به قرمز رنگ تغییر داده شد. با این تغییر، شناسایی پشههای مقاوم به راحتی امکانپذیر بود. با این ابزار با تعداد کمی محرک ژنی ضد مالاریا جمعیت آنها در طول زمان افزایش مییابد. پس به احتمال زیاد بتوان با روش محرک ژنی، بیماری مالاریا را ریشهکن کرد. همچنین میتوان بیماریهای دیگر مانند تب زرد و تب دنگی را از بین برد.
با ابزار قدرتمند ژن درایو میتوان صدها گونه بومی را که در معرض انقراض قرار دارند برگرداند. اما به همین جا ختم نمیشود. اگر محرکهای ژنی حتی به صورت تصادفی رها شوند میتواند در گونه موردنظر تغییرات سریعی ایجاد کند. حتی ممکن است یک گونه را به طور کامل منقرض کند. آخرین نگرانی این است که مهندسی ژنتیکی و ایجاد محرکهای ژنی در هر آزمایشگاهی امکانپذیر است. پس میتواند برای بشریت و طبیعت هشدار بزرگی باشد اگر دانشمندان مسئولانه و محتاطانه عمل نکنند.
باید گفت محرکهای ژنی برای همه گونهها امکانپذیر نیست و تنها برای گونههای با قابلیت تولیدمثل ممکن است. بنابراین مهندسی ژنتیکی برای ویروسها و باکتریها قابل استفاده نیست. از سوی دیگر گسترش یک صفت ژنتیکی تنها از نسلی به نسل دیگر انجام میشود. پس تغییر یک جمعیت یا حذف یک گونه وقتی سریع اجرا خواهد شد که چرخه تولیدمثل گونه سریع باشد مانند حشرات و موشها و ماهیها. در انسان یا فیل قرنها طول میکشد که یک صفت ژنتیکی گسترش یابد.
همیشه بیخطرترین گزینه حفظ وضعیت موجود نیست. محرکهای ژنی خطرهایی دارند، اما در حال حاضر بیماری مالاریا وجود دارد و هر روز هزار نفر را میکشد. استفاده از فناوری کریسپر و ژن درایو میتواند ترسناک باشد، اما گاهی اقدام نکردن بدتر است.
در زمینه فناوری ویرایش ژنتیکی CRISPR بیشتر بخوانید:
>>انجام نخستین آزمایش ویرایش ژن CRISPR روی یک انسان
منبع: TED
استفاده و بازنشر مطالب تنها با ذکر لینک منبع و نام (مجله فناوریهای توانافزا و پوشیدنی) مجاز است