در مورد شرایط وخیم پزشکی، سرطان و شرایطی که بیمار به جراحی پیچیده نیاز دارد، سلامت فیزیکی بیمار و روحیه او تا حد قابل توجهی ضعیف شده است. جراحی باز و تهاجمی و یا روند سخت و خشن برخی جراحیها را میتوان تا حد ممکن کاهش داد. به این شکل هم روند بهبود بیمار و هم روحیه وی بهتر خواهد بود. استفاده از فناوری رباتیک این امر را میسر میسازد. سامانههای رباتیک بسیاری هم اکنون نیز در دسترس پزشکان هست. اما به دلایلی مانند جا افتادن روشهای پیچیده درمان از این ادوات استفاده نمیشود. در ادامه این مقاله از مجله فناوریهای توان افزا و پوشیدنی به مرور رباتهای پیشرفته پزشکی میپردازیم.

امکانات رباتیک جراحی وجود دارند؟
آیا یک جراح قلب میتواند بدون باز کردن سینه بیمار روی یک قلب تپنده جراحی کند؟ آیا یک ربات باریک میتواند درون رگها، مویرگها یا نایچههای بیمار حرکت کند، در مکان مورد نظر حالت منعطف خود را به ساختاری محکم تغییر بدهد و جراحی را انجام دهد؟ یا یک میدان مغناطیسی را میتواند برای حرکت یک ربات پاکسازی کننده داخل رگها به کار برد؟
Pierre Dupont طراح سامانههای رباتیک پزشکی است. به گفته وی این تجهیزات هم اکنون نیز پیشقراول تجهیزات پزشکی هستند. رشته وی در واقع مهندسی تجهیزات دقیق برای وارد شدن به بدن بیمار است. این تجهزات تصویربرداری، تشخیص و درمان را انجام میدهند. تجهیزاتی با محوریت بیمار برای کنترل شرایط دیابت و قند خون و پوشیدنیهای کمکی قربانیان سکته مغزی نیز در همین رشته طراحی میشوند.
درمان نای و مسیر گوارش منفصل
کارمندان آزمایشگاه Dupont در بیمارستان کودکان بوستون پژوهشگران پسی دکتری یا دانشجویان تحصیلات تکمیلی هستند. Dupont در این آزمایشگاه آموخت که از هر سه هزار نوزاد سالانه یکی با مری منفصل متولد میشود. در واقع گلوی آنان به یک کیسه بسته منتهی میشود. شکم نیز یک سری مسدود دارد. اگر فاصله بین این دو مسیر بیشتر از چند سانتیمتر باشد، امکان دوختن دو مسیر به یکدیگر وجود ندارد چراکه بخیهها پاره میشوند. سالانه ۱۵ تا ۲۰ نوزاد با این شرایط حاد به دنیا میآیند. برای مداوای آنان معمولا نوزاد باید سه ماهه باشد. درمان نیازمند بیحسی و سرکردن اعضای بدن به مدت چند هفته در بخش مراقبتهای ویژه است. جراح به مرور باید بخیهها و محل اتصال را محکم کند. میلیمتر به میلیمتر. به این شکل بافت ناحیه مورد نظر رشد میکند. نواحی کوتاه رشد میکنند و امکان اتصال آنان به یکدیگر فراهم میشود.
مدت زمان زیاد بی هوش و خطرات بسیار آن برای مغز نوزادان
اما در این زمان برای مغز کودک چه اتفاقی میافتد؟ زمانی تا حد طولانی در بخش مراقبتهای ویژه؟ در حالی که برخی پژوهشگران روی رشد بافت لازم برای ترمیم در آزمایشگاه تمرکز دارند این شرایط به نظر قابل تغییر میرسد. به گفته Dupont تنها با داشتن مقداری بافت اضافی از بدن با شرایط خاص میتوان یک رباتی را برای ایجاد نیروهای انقباضی مناسب به کار گرفت. این نیروها را بافت را به رشد تحریک میکند. جراحی رشد بافت هم از همین اصل پیروی میکند اما عملیات وحشتناکی است.
بنابران Dupont تصمیم گرفت که یک ربات لوله مانند بسازد که به طور موقت این فضای خالی بدن را پر کند و همزمان بافت را هم تحریک کند. این روش به کودک اجازه میدهد هوشیار و فعال باقی بماند. با آزمایش این روش روی خوکها، جاندار کاملا هوشیار بود و توانست با این دستگاه غذا بخورد. این ربات به علت هزینههای بالای آزمایش نسبت به تعداد بیماران به آزمایش انسانی نرسید. با این حال وجود آن نشان دهنده توانایی بالایی مهندسی برای جراحی رباتیک در بهبود وضعیت بیمار و روشهای جراحی است.
چطور یک ربات جراح نرم، محکم می شود؟
به گفته Dupont پژوهشگران حوزه رباتیک در اصل مخترع هستند. آنان همواره در لبه فناوری هستند. این افراد در پی انجام کاری نیستند که سایرین انجام میدهند. آنان در پی چیزی غیرمتعارف هستند. Dupont به شخصه بیان کرد که نظر فعالان پزشکی مبنی بر احمقانه بودن ایدههایش او را به ورود به بیمارستان تشویق کرد. او قصد داشت چیزی بسازد که کاربرد واقعی در پزشکی داشته باشد.
Dupont یک متخصص در حوزه رباتیک پزشکی و رباتیک جراحی است. وی و کارمندانش به تازگی در مجله Science یک مقاله مروری در مورد مقالات ازدیاد این حوزه چاپ کردند. در واقع کمتر از ۱۰ مورد در سال ۱۹۹۰ و بیش از ۵۲۰۰ مورد در سال ۲۰۲۰ مقاله وجود داشته است. مشوق هشتاد درصد این پژوهشها در ۱۰ سال گذشته پذیرش تجهیزات رباتیک در حوزه سلامت بوده است. به عقیده Dupont بسیاری از مهندسین حوزه رباتیک طرحی ظریفتر از دستگاههای موجود دارند که دقیقا همان کار را انجام میدهد.
عدم پذیرش میلی بات های مغناطیسی
یک مثال از فعالیتهای خود Dupont توسعه روشی برای سوق دادن رباتهای شبه خودکار در بدن با میدان مغناطیسی دستگاه MRI است. فناوری نانوباتهای پزشکی(مقاله کاربرد نانوربات ها در پزشکی) قبلا هم حضور داشتند اما این فناوری جدید امکانات خاصی دارد. این روش میتواند میلیباتهای ساخته شده از آلیاژ استیل به قدر کافی برای شکافتن سدهای ایجاد شده داخل رگها سریع هستند. فناوری شکافت بافت نرم با کمک نیروی الکترومغناطیسی را میتوان برای درمان به مکانهای دور از دسترس در بدن نیز به کار برد. به طور مثال برای دسترسی به مایع مغز در بیماران مبتلا به hydrocephalus(ازدیاد غیر طبیعی مایع) به کار برد. این شرایط میتواند سبب فوت به
علت افزایش فشار شود. اما درمانهای جا افتاده مانند بالون زدن برای باز کردن مسیر رگ مانع مهمی در گسترش روشهای جدید هستند.
ربات های پیوساتر و جراحی مغز
از اختراعات مهم Dupont میتوان به رباتهای پیوسته یا Continuum Robots اشاره کرد. این رباتها برای حرکت داخل مسیرهای پیچیده و منحنی بافت زنده طراحی شده است. رباتهای سنتی قسمتهای سخت دارند که با مفاصلی به هم وصل میشوند. برای حرکت داخل بدن این اتصالات سخت بازدهی ندارند. یک ربات پیوسته با بینهایت مفصل بهترین راه حل است. فناوری این رباتها شبیه آنتن رادیو تلسکوپ است. Dupont در دوره پسی دکتری در دانشگاه Harvard روش شبیه سازی ریاضی برای مدل کردن این رباتها را به خوبی آموخت. این رباتها یک خمیدگی ذاتی دارند که به کمک آن نوک ربات را به صورت کشسان هدایت میکنند. هدایت و مهندسی ربات به دقت بالا امکان پذیر است.

نخستین ربات از این نوع، بنا به درخواست یک جراح مغز و اعصاب ساخته شد. این جراح به Dupont گفت که آزادی عمل با دوبازی رباتیک در جراحی از طریق یک حفره باریک در مغز بیشتر از یک بازو است. در واقع یک حفره کوچک در مغز ایجاد میشود و تومور با رباتی باریک جراحی میشود. بنابراین Dupont سامانهای طراحی کرد که جراح به کمک سر انگشتان خود آن را هدایت میکرد. این سامانه برای ۲۰هزار جراحی تومور مغزی در سال استفاده میشود. همچنین پتانسیل به کارگیری در جراحیهای دیگر را نیز داراست.
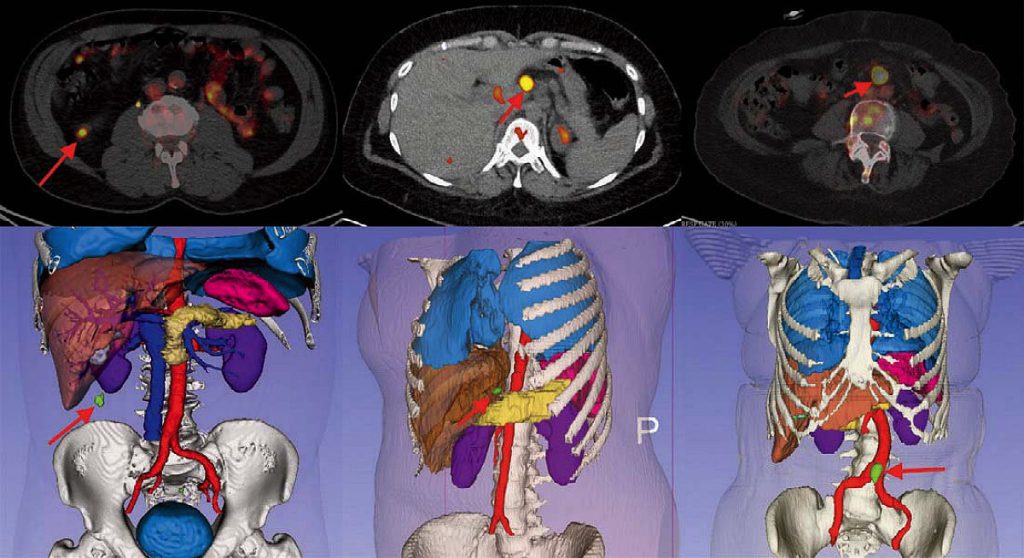
رباتیک جراحی برای برداشتن تومور سرطانی با تصویربرداری دقیق
اجرای جراحی با کمینه تهاجم با کمک رباتها ممکن است. این روش به کاهش دوره نقاهت بیماری هم کمک میکند. با توجه به اینکه این جراحیها از طریق یک حفره کوچک انجام میشوند باید روشهایی برای بهتر کردن دید جراح در نظر گرفت. Jayender Jagadeesan دانشیاری است که در بیمارستان زنان Brigham به این کار مشغول است. وی در حال توسعه رباتهایی است که روشهای مختلف تصویربرداری در لحظه( مانند لاپاروسکوپی استریو، MRI، CT اسکن و تصویر برداری فراصوت) را با روشهای مختلف جراحی ترکیب میکند. نتیجه ایجاد تصویری سه بعدی در لحظه است که دقیقا حرکات ربات را داخل بدن نشان میدهد.
در طول جراحی خون، دود و مشکلات روشنایی هست و ساختار آناتومی کلیدی معمولا در پس بافت قابل مشاهده پنهان شده است. پس باید دید جراح را بهبود بخشید
Jayender Jagadeesan
وی روشی برای تشخیص تومورهای زیرسطحی ابداع کرده است که مکان تومور و مرزهای آن را دقیقا مشخص میکند. در واقع در حین جراحی تشخیص مرز تومور دشوار است. اینکار معمولا با لمس بافت توسط جراح انجام میشود. اگر مرز بافت تومور به اندازه کافی برداشته نشود، سلولهای خطرناک در بدن باقی میمانند. مسلما حالت ایده ال تهاجم هرچه کمتر به بافت سالم است. روش وی دقیقا اندازه و شکل تومور را در سه بعد نشان میهد. در نتیجه جراح برای سوزانیدن تومور راحتتر تصمیم میگیرد.
سامانه ردیابی Jagadeesan در جراحیهایی برای برداشتن نودهای لنفی خطرناک، سرطان کلیه، سرطان تیروئید و پاراتیروئید به کار گرفته شده است. این روش به خصوص در جراحی سرطان ریه مفید است. روش استاندارد کنونی برداشتن کل لوب تنفسی است که ظرفیت ریه را کم میکند. ولی با روش Jagadeesan تنها خود بافت تومور خارج میشود. با توجه به شرایط وخیم بیماران سرطانی و روشهای سخت درمان، کم کردن آسیب به بدن هنگام درمان بسیار مهم است. کاربردهای کلی این سامانه در مرحله آزمایشی است.
ربات های بینا و حساس
یکی از دانشجویان پسی دکتری Jagadeesan با نام Ruisi Zhang روی بازخورد لمسی رباتهای جراح کار میکند. نخستین چالش گروه ثبت بافت و سختی سطوح است. به گفته Ruisi Zhang قدرت حس لاسمه خانمها و آقایون متفاوت است. همچنین حساسیت حس لامسه در سنین مختلف تفاوت دارد. بنابراین نوک وسیله رباتیک باید قابل تنظیم باشد. این وسیله با لرزش و سیگنالهای فرکانس پایین کار میکند. نیروهای کم فرکانس برای تشخیص لیزی، سختی و شکل کلی شیئ به کار میرود. لرزش نیز برای تشخیص بافت سطح به کار میرود.
به نظر Ruisi Zhang بازخورد لمسی هنر ایجاد توهم لامسه است. به گفته وی در حال حاضر توانایی ایجاد هر حس لامسهای که توسط جراح قابل فهم باشد فراهم نیست. زیرا هنوز همه بازخوردهای دریافتی را نمیتوان به لامسه ترجمه کرد. اما او امیدوار است که با کمک سایر پژوهشگران توسعه دستگاههای قابل استفاده برای انواع مختلف بافت و عضو بدن ممکن باشد. به این شکل جراحان از بهبود کیفیت جراحی رباتیک استفاده خواهند کرد و روند بهمبود بیمار سریعتر میشود.
کاربرد فناوری های نوین در بهبود خدمات بهداشت و درمان
پیش بینی تغییرات جراحی رباتیک در آینده
ده ربات پزشکی و ربات جراح مهم
منبع: harvardmagazine
«استفاده و بازنشر مطالب تنها با ذکر لینک منبع و نام (مجله فناوریهای توان افزا و پوشیدنی) مجاز است.»