پژوهشگران مهندسی مکانیک MIT در حال توسعه روشهای جدید و ابتکاری برای بهبود مراقبتهای بهداشتی و سلامت هستند. این پژوهشگران با دیدی مکانیکی به مسائل پزشکی نگاه میکنند و در حال توسعه روشهای جدید و نوآورانه برای درک عمیق ما از بیماری و توسعه راهکارهای جدید برای درمان آن هستند. برای آشنایی با دیدگاه مهندسان مکانیک در مورد بدن انسان و انواع بیماریها با مجله فناوریهای توانافزا و پوشیدنی همراه باشید.
سلول های بنیادی
در سال ۲۰۰۶ برای نخستین بار پژوهشگران سلولهای بنیادی را بدون استفاده از جنین ایجاد کردند. در این روش سلولهای پوستی بالغ دوباره برنامهریزی میشوند تا تبدیل به سلولهای بنیادی پرتوان (pluripotent stem cells) یا iPSCs شوند. این سلولها میتوانند برای استفاده در تقریباً هر قسمت از بدن، از کبد تا قلب یا مغز متفاوت باشند. با این روش مناطقی که به موجب بیماری آسیب دیدهاند میتوانند دوباره بهبود یابند.
اما پس از بیش از یک دهه پژوهش در مورد iPSCs، روند ایجاد آنها هنوز بسیار ناکارآمد است. پروفسور Domitilla Del Vecchio میگوید: «ما متعجبیم که پس از ۱۰ سال پژوهش در این زمینه، کارایی برنامهریزی مجدد iPSC هنوز تنها ۰٫۱ درصد است. و هنوز در مرحلهای نیست که شما بتوانید از آن برای اهداف بالینی استفاده کنید».
Del Vecchio و همکارانش امیدوارند که این روند را تغییر دهند. در حال حاضر پژوهشگران iPSCها را با ارائه DNA ترکیبی به هسته یک سلول سوماتیکی (somatic) همچون سلول پوستی تولید میکنند. این DNA مصنوعی سطح بالایی از پروتئینهای انتخابی را به نام فاکتور رونویسی ژنتیکی (transcription factor) تولید میکند که هدف آن سوق دادن سلولهای سوماتیکی به سمت برنامهریزی مجدد سلولهای بنیادی است. اما بارگذاری بیش از حد یک سلول با چنین سطح بالایی از فاکتور رونویسی ژنتیکی منجر به یک روند بسیار ناکارآمد میشود. Del Vecchio میگوید: «اگر شما یک سامانه مکانیکی همچون یک ماشین یا بازوی رباتیک داشته باشید و آن را تحت فشار قرار دهید، نباید انتظار داشته باشید که سامانه دقیقاً انتظارات شما را برآورده کند».
Del Vecchio و گروهش برای حل این مشکل یک شتاب دهنده و ترمز به روند افزودند. آنها با استفاده از تجزیه و تحلیل ریاضی میتوانند نشان دهند که با یک تعادل میتوان به حالت مناسب سلولهای بنیادی چندگانه دست پیدا کرد. با کمک مولکولهای کوچک، DNA مصنوعی که از طریق یک ویروس تهیه میشود میتواند سطح قابل تنظیم فاکتورهای رونویسی را بر اساس یک پیکربندی هدف تولید کند. این روش که کنترل کننده بازخورد ژنتیکی مصنوعی نامیده میشود، میتواند غلظت فاکتورهای رونویسی در سلول را به نقطهای هدایت کند که تبدیل به یک سلول بنیادی شود.
برنامههای کاربردی Del Vecchio ممکن است پیامدهای وسیعی برای نحوه درمان بیماریها داشته باشد. پژوهشگران میتوانند به سرعت سلولهای قلب سالم را برای بیماران مبتلا به بیماری قلبی یا سلولهای بتا را برای بیماران دیابتی ایجاد کنند. همچنین پزشکان میتوانند سلولهای بنیادی را به سرعت ایجاد کنند تا بیماریهای بسیاری درمان شود. گروه پژوهشی Del Vecchio نشان دادند که چگونه پژوهشگران مهندسی مکانیک در حال توسعه روشهای جدید و نوآورانه برای درک عمیق ما از بیماری و توسعه راهکارهای جدید برای درمان آن است.
تشخیص بیماری
درک بیماری با سلول آغاز میشود. استادیار Ming Guo، علاقهمند به رمزگشایی خواص مکانیکی سلول سالم و بیمار به عنوان راهی برای توسعه یک ابزار تشخیصی است. Guo میگوید: «تنها با نگاه کردن به یک سلول سالم و مقایسه آن با یک سلول بیمار، میتوان گفت که آنها از لحاظ مکانیکی متفاوت هستند».
استحکام یک ویژگی کلیدی در تشخیص نوع بیماری سلول است. برای نمونه نشان داده شده که سلولهای سرطانی نرم هستند در حالی که سلولهای آسم اغلب سفت هستند. Guo و همکارانش در حال حاضر یک روش ایمن و کمتر تهاجمی برای تجزیه و تحلیل مکانیکی یک سلول برای کمک به تشخیص بیماری با استفاده از یک میکروسکوپ نوری استاندارد ایجاد کردهاند.
Guo میگوید: «ما دریافتیم که نوسانات فرکانس بالا میتواند به ما کمک کند که سفتی سلول را اندازه گیری کنیم و مکانیک آن را درک کنیم». درک این خواص مکانیکی میتواند به پزشکان کمک کند بیماری را براحتی تشخیص دهند. Guo در حال همکاری با پزشکان در بیمارستان عمومی ماساچوست در استفاده از این روش برای تشخیص سرطان و آسم است. امید است که پزشکان و پژوهشگران بتوانند اثربخشی دارو را با اندازهگیری ویژگیهای مکانیکی سلول پیش و پس از درمان بررسی کنند.
ردیابی بیماری
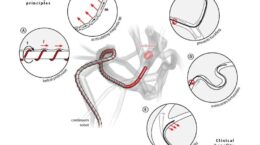
در حالیکه بهبود روشهای تشخیصی میتواند در درک بیماری مؤثر باشد، ردیابی چگونگی رشد بیماری میتواند کلیدی برای توسعه مداخلات درمانی جدید باشد. Roger Kamm ، پروفسور برجسته Cecil و Green Distinguished است. او و آزمایشگاهش از دستگاهی استفاده میکنند تا سلولهای تومور را زمانی که شبکهی عروقی را ترک میکنند و در نهایت به تومور تبدیل میشوند، ردیابی کنند. این دستگاههای microfluidic کوچک میتواند به ما کمک کند چگونگی گسترش سرطان را درک کنیم.
دستگاههای Microfluidic به Kamm اجازه میدهد نیروهایی که نشان دهنده رفتارهای سلول سرطانی است را تجزیه و تحلیل کند. درک تعامل نیروها بین سلولهای اندوتلیال (endothelial) و سلولهای تومور، اهداف بالقوه درمانی برای پیشگیری یا به حداقل رساندن گسترش سلولهای سرطانی است. این دانش میتواند فرصتهای جدیدی در درمان سرطان و حتی توسعه روشهای جدید ایمنی باز کند.
درمان بیماری
پژوهشگران با شناخت بیشتر از چگونگی رشد و گسترش بیماریها قادرند روشهای جدیدی برای درمان بیماریها توسعه دهند. در میان آنها Ellen Roche است که روش منحصر به فرد دوگانهای برای درمان بیماریهای قلبی با استفاده از درمانهای مکانیکی و بیولوژیکی دارد. Roche میگوید: «ایده این است که به صورت مکانیکی به قلب کمک کنیم. و تنها از یک روش زیست تقلیدی برای کمک و تقویت آن بهره بریم».
Roche با استفاده از روشهای جدیدی همچون رباتیک نرم به دنبال توسعه دستگاههایی است که خواص بافت قلب و حرکت آن را تقلید میکند. چنین دستگاهی در اطراف قلب پیچ میخورد تا به پمپاژ کمک کند. Roche میگوید: «با طراحی هوشمندانه کانالهای ساده سیالات و تقویت مواد نرم میتوان این حرکت بسیار پیچیده (پمپاژ) را تنها با تغییرات الاستومری و فشار هوا و یا آب به دست آورد».
Roche در حال کار بر روی درمانهای مکانیکی برای درمان بیماریهایی همچون بیماریهای قلبی مادرزادی و حملات قلبی است. او و گروهش در حال توسعه دستگاههای هوشمندی هستند که تحویل محلی دارو را به جای تحویل داروهای سیستمیک ارائه میدهند. Roche میگوید: «یکی از اهداف اصلی من این است که ترکیب این روشهای مکانیکی و بیولوژیکی و نحوه ارتباط آنها با یکدیگر را درک کنم». درک چگونگی تعامل این درمانهای مختلف میتواند بهترین نتیجه را برای بیشترین کارایی به همراه داشته باشد.
توانبخشی
پژوهشگران در حال توسعه ابزارهایی هستند تا به فرآیند بازیابی در مواردی که بیماری در طول زمان تشخیص یا درمان نشده، کمک کنند. مهندسان مکانیک در حال یافتن روشهایی برای بهبود کیفیت زندگی افراد پس از بیماری هستند. این روشها شامل بهینهسازی طراحی پروتزهای پا یا ساخت صندلیهای چرخدار ارزانتر است. این کار همچنین شامل ابزار و وسایلی است که میتواند در توانبخشی فیزیکی مورد استفاده قرار گیرد. یکی از این ابزار MIT-MANUS است. MIT-MANUS یک ربات است که توسط پروفسور Neville Hogan ساخته شده است تا قربانیان سکته مغزی بهبود یابند و توان حرکت خود را دوباره بدست آورند.
هیچ دو بیمار سکته مغزی مشابه هم نیستند و این مسئله موجب پیچیدگی بیشتر مسئله میشود. Hogan با متخصصان مغز و اعصاب و دانشمندان علوم اعصاب در درک فرآیند بازتوانی و کنترل حرکتی مغز همکاری داشته است. او با استفاده از این دانش در تلاش است رباتهایی توسعه دهد که با بیماران سکته مغزی ارتباط برقرار و به آنها کمک میکند تا کنترل حرکتی خود را دوباره به دست آورند.
در ابتدا MIT-MANUS برای کمک به بازگرداندن عملکرد حرکتی شانهها و آرنج بیماران سکته مغزی طراحی شده بود. بیماران دست و پای خود را به یک بریس و سپس به بازوی رباتیک وصل میکنند. بیماران باید یک کنترلر متصل به صفحه نمایش ویدئویی را در دست گیرند. یک بازی ویدیویی بیماران را تشویق میکند تا دست و مچ دست خود را حرکت دهند. MIT-MANUS حرکات بیمار را هدایت و به آن کمک میکند. سپس ربات این اطلاعات را برای پزشکان و متخصصان فیزیکی ذخیره میکند.
ساخت رباتی همچون MIT-MANUS برای کمک به توانبخشی قربانیان سکته مغزی، ردیابی حرکتهای کوچک در سلولها و یا استفاده از مدارهای ژنتیکی برای ایجاد سلولهای بنیادی همه نشان دهنده این است که مهندسان مکانیک در حال شکل دادن درک اصلی ما از بیماری و نحوهی درمان آن هستند.
بیشتر بخوانیم:
>>راهکارهای نوآورانه توانبخشی برای کمک به قربانیان سکته یا آسیب نخاعی
>>تشخیص سریع بیماریها با ساخت توالی سنج ارزان و دقیق DNA
منبع: news.mit.edu
«استفاده و بازنشر مطالب تنها با ذکر لینک منبع و نام (مجله فناوریهای توان افزا و پوشیدنی) مجاز است.»