استفاده از ژن درمانی برای مقابله با ویروس HIV از سال ۲۰۰۷ و پس از درمان کامل یک بیمار حامل HIV در آلمان از اهداف بسیاری از پزشکان بوده است. در سال ۲۰۱۷ در چین روش CRISPR برای درمان بیماری حامل این ویروس که مبتلا به سرطان خون بود به کار گرفته شد. برای آشنایی بیشتر با این پژوهش و تاریخچهی ژندرمانی برای مقابله با HIV با این نوشتار از مجلهی فناوریهای توانافزا و پوشیدنی همراه باشید.
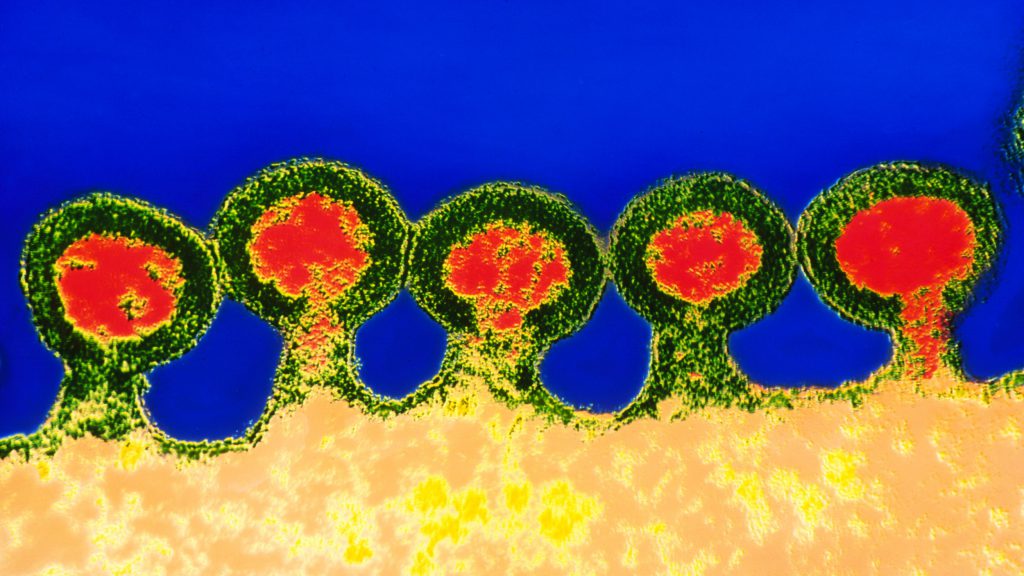
فرد بیماری را تصور کنید که برای آگاهی از وضعیت سلامت خود به بیمارستان مراجعه میکند. پس از روزها انتظار و انجام آزمایشهای مناسب درمییابد که یک بیمار HIV مثبت است. و نه تنها این ویروس در بدن وی حضور دارد، بلکه مبتلا به سرطان خون نیز هست.
آزمایشی برای مبارزه با HIV در چین
حتی در بهترین شرایط روحی، روبهرو شدن با این شرایط دشوار است. خصوصا در کشورهایی که جامعه شدیدا بیماران HIV مثبت را پس میزند. این شرایط برای مرد جوانی در کشور چین رخ داده است. وی یکی از افرادی است که برای انجام آزمایشهای انسانی ژندرمانی به کمک CRISPR برای درمان عفونت ویروسی و سرطان به شکل همزمان واجد شرایط شناخته شده است.
در ماه ژولای سال ۲۰۱۷ پزشکان با شیمیدرمانی و پرتودرمانی مغز استخوان وی را تحت درمان قرار دادند. به این صورت امکان تزریق سلولهای بنیادی به مغزاستخوان فراهم شد. این سلولهای بنیادی توسط فردی سالم برای درمان اهدا شده بود. امید این بود که جایگزینی این سلولها با سلولهای فرد بیمار امکان درمان سرطان را فراهم کند. این سلولهای بنیادی توسط ابزار CRISPR دستکاری شده بود. هدف از کار انداختن ژنی با نام CCR5 بود. بدون این ژن ویروس HIV نمیتواند به بدن حمله کند.
اکنون پس از گذشت دو سال بیمار به لحاظ جسمی مشکل خاصی ندارد و سرطان وی در حال بهبودی است. سلولهای بنیادی تزریق شده کارآمد باقی ماندند و بدن وی را با خون و سلولهای حیاتی سیستم ایمنی تغذیه میکنند. درصد اندکی از این سلولها جهش CCR5 را نیز حفظ کردهاند. بیماری HIV همچنان در بدن این فرد وجود دارد و برای کنترل ویروس دارو مصرف میکند. با این وجود این پژوهش نشان میدهد که فناوری CRISPR برای استفاده روی انسان ایمن است.
اهمیت این پژوهش
بر اساس نظر یک پژوهشگر فعال در درمان سرطان به نام Carl June ویرایش ژنتیکی انجام شده در این عملیات دقیق است و سلولهای دستکاری شده سامانهی ایمنی را برانگیخته نمیکنند. هر چند نمیتوان بر اساس درمانی انجام شده روی یک بیمار نظر قطعی داد، این پژوهشها امید بخش به نظر میرسد.
یکی از جنبههای مهم این پژوهشها سرعت زیاد است. فاصلهی زمانی آزمایش انسانی و آزمایشهای درمان HIV روی موشها بسیار کم و تنها دو سال بوده است. در پژوهشی از دانشگاه Pennsylvania یک درمان سرطان با نام CAR-T توسعه داده میشود. این درمان شامل دستکاری ژنتیکی سلولهای ایمنی بدن برای تبدیل آنها به شکارچیان سلولهای سرطانی است. در این پژوهشها پنج سال طول کشید تا تست انسانی پس از تست حیوانی آغاز شود.
تاریخچه ی مبارزه با HIV به کمک ژن درمانی
این آزمایش نخستین نمونه برای کنترل HIV به کمک ژندرمانی است. پژوهشگران بیش از یک دهه برای یافتن راهی که ژن CCR5 را غیرفعال نماید، تلاش نمودهاند. این پژوهشها در سال ۲۰۰۷ آغاز شده است. در سال ۲۰۰۷ یک پزشک آلمانی یک بیمار HIV مثبت مبتلا به سرطان خون را برای آزمایشی مشابه انتخاب کرد. این بیمار از یک اهدا کنندهی خاص سلولهای مغز استخوانی دریافت کرد که به صورت طبیعی جهش خاص داشت. به واسطهی این جهش اهدا کننده در برابر سلولهای HIV مقاوم بود. این بیمار نخستین نمونهی کاملا درمان شدهی HIV مثبت بوده است.
این تجربه پزشکان را به نابودی کامل ویروس HIV امیدوار کرد. نخستین آزمایش ژندرمانی برای درمان HIV در سال ۲۰۰۹ شرکتی در کالیفرنیا به نام Sangamo Therapeutics انجام شد. این آزمایش شامل دستکاری ژنتیکی سلولهای نوع T بود، اما نتایج آن امیدبخش نبود. سلولهای نوع T در سیستم دفاعی بدن نقش کنترل کننده را دارند.
راه بهتر دستکاری ژنتیکی سلولهای سازندهی سلولهای نوع T و سایر گلوبولهای سفید است. این سلولها در مغز استخوان قرار دارند. دستیابی و دستکاری آنان دشوارتر است اما گزینهی مناسبتری هستند. در صورت موفقیت با این روش بیمار منابع کافی برای مبارزه با HIV در خون و سیستم ایمنی خود خواهد داشت. این روشی است که CRISPR پی خواهد گرفت.
کارایی CRISPR در مبارزه با HIV
گروهی پژوهشی در چین سلولهای دستکاری شدهی انسان با جهش مناسب CCR5 را با موفقیت روی موش آزمایش کرده بود. در بهار سال ۲۰۱۷ این گروه آزمایشی در ۳۰۷ بیمارستان در پکن را برنامهریزی کرد. تا کنون پزشکان تنها یک بیمار را برای این درمان پذیرفتهاند، اما در صورت اثبات کارآمد بودن این روش، بیماران بیشتری پذیرفته خواهند شد.
Hongkui Deng ریاست مرکز پژوهش سلولهای بنیادی بیمارستان Peking برای دستکاری سلولهای بنیادی آنان را تحت یک شوک الکتریکی قرار میدهد. پس از آن اجزای CRISPR از دیوارهی سلول عبور کرده و وارد عمل میشوند. این اجزا شامل یک آنزیم برای بریدن DNA و یک راهنما برای تعیین مکانهای مناسب برش است. در این روش CRISPR برای زمان کوتاهی داخل سول است. پس امکان مشاهدهی ناهنجاری در بریدن DNA کاهش مییابد. و به همین دلیل خطا کاهش مییابد. البته زمان کوتاه ساکن شدن در سلول به معنای افزایش تعداد سلولهای دستکاری شده نیز هست.
به صورت ایدهآل دو کپی از CCR5 باید به کلیهی ۱۶۲ میلیون سلول بنیادی وارد شود. این شرایطی است که در مورد بیمار درمان شده در آلمان نیز وجود داشت. اما در عمل تنها ۸.۳ از سلولهای مغزاستخوان حداقل یک کپی از CCR5 را داشت. در این پژوهش تعداد سلولهای حامل دو کپی از CCR5 ذکر نشده بود.
این تعداد پس از ۱۹ ماه رصد وضعیت بیمار پایدار مانده است. اما سوال مهمتر مربوط وضعیت سلولهای نوع T در بدن بیمار است. آیا سلولهای نوع T نیز این دستکاری را دریافت نمودهاند؟ تنها در دو درصد از نوع خاصی از این سلولها که مورد حملهی HIV قرار میگیرد، اجزای CCR5 یافت شد. این میزان نباید تاثیری در کاهش تعداد سلولهای HIV داشته باشد.
در نهایت موفیت ژندرمانی به بازده روش دستکاری ژن بازمیگردد. در سال گذشته در نتیجه دستکاری ژنتیکی جنین انسان برای مقاوم سازی جنین در برابر HIV چین خواستار قوانین محکمتری برای استفاده از ژندرمانی در انسان شده است. این تجربه پژوهشهای انجام شده در زمینهی ژندرمانی را تحت تاثیر قرار خواهد داد و حساسیتهای را در هنگام ارائهی کار در مقابل عموم مردن افزایش میدهد. اما پژوهشی که در این مقاله به آن اشاره شد، با موافقت یک بیمار بزرگسال انجام شده است. لازم به ذکر است افرادی که در کلیهی سلولهای بدن خود ژن CCR5 را نداشته باشند بیش از سایرین در معرض بیماریهایی مانند آنفلانزا هستند و طول عمری کمتری نسبت به سایرین دارند.
بیشتر بخوانیم:
از بین بردن موقتی احساس درد با فناوری CRISPR
انجام نخستین آزمایش ویرایش ژن CRISPR روی یک انسان
منبع: wired.com
«استفاده و بازنشر مطالب تنها با ذکر لینک منبع و نام (مجله فناوریهای توانافزا و پوشیدنی) مجاز است»